Neue Empfehlungen zur Standardprophylaxe
Durch die Entwicklung neuer antiretroviraler Medikamente konnte die Verträglichkeit verbessert und zudem die Häufigkeit und Intensität von Nebenwirkungen verringert werden. Als Standardprophylaxe wird nun folgende Medikamentenkombination empfohlen:
Isentress 1 Tablette zweimal täglich
plus
Truvada 1 Tablette einmal täglich über 28 bis 30 Tage:
- Standard
- Raltegravir + Tenofovir-DF/Emtricitabin entspricht: Isentress® + Truvada®
- Dosierung:
- Isentress 400 mg 1 – 0 – 1 +
- Truvada 245/200 mg 1 – 0 – 0
- Alternativen
- Alternativ zu Isentress® (Raltegravir) kann Kaletra® (Lopinavir/Ritonavir), alternativ zu Truvada® (Tenofovir-DF/Emtricitabin) kann Combivir® (Zidovudin/Lamivudin) eingesetzt werden.
- Dosierungen:
- Kaletra 200/50 mg 2 – 0 – 2
- Combivir 300/150 mg 1 – 0 – 1
Eine Modifikation des Prophylaxeschemas kommt z. B. bei bekannten Medikamenten-resistenzen des HIV-positiven Indexpatien-ten oder auch bei Schwangerschaft der betroffenen Mitarbeiterin oder Medikamentenunverträglichkeiten in Betracht.
Indikation zur HIV-PEP
In der neuen Leitlinie findet sich folgende Stellungnahme: „Wird die mit HIV infizierte Indexperson erfolgreich mit antiretroviralen Medikamenten behandelt (d. h. Viruslast bei der letzten Kontrolle unter 50 Viruskopien/ml, kontinuierliche Einnahme der Medikamente), muss bei akzidentellen Verletzungen und bei Sexualkontakten nicht mit einer übertragungsrelevanten Exposition gerechnet werden“ (DAIG 2013, s. „Weitere Infos“).
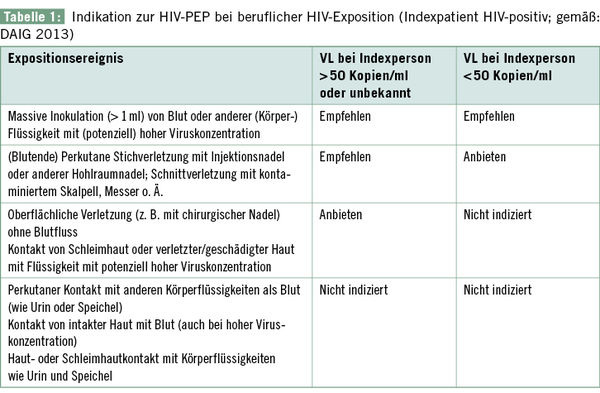
Die Indikation zur HIV-PEP bei beruflicher HIV-Exposition wird gemäß der neuen Leitlinie nach Tabelle 1 dargestellt.
Eine im September 2013 veröffentlichte US-amerikanische Leitlinie zur HIV-PEP kommt zu folgendem Schluss: „Exposure to a source patient with an undetectable serum viral load does not eliminate the possibility of HIV transmission or the need for PEP and follow-up testing. While the risk of transmission from an occupational exposure to a source patient with an undetectable serum viral load is thought to be very low, PEP should still be offered” (Kuhar et al. 2013).
Hintergrund hierfür ist die Tatsache, dass die Viruslast im Plasma lediglich den Level des zellfreien Virus im peripheren Blut beschreibt, es konnte jedoch nachgewiesen werden, das HIV in latent infizierten Zellen trotz antiretroviraler Therapie persisiert und das es so unter Umständen zur Virustransmission kommen kann (Kuhar et al. 2013).
Vor dem Hintergrund der amerikanischen Leitlinie und der Tatsache, dass es keine Literatur zum fehlenden Übertragungsrisiko bei berufsbedingten Blutkontakten mit Indexpatienten mit < 50 HIV-Kopien/ml gibt, sondern das lediglich Analogieschlüsse zu diskordanten Paaren gezogen werden können (Cohen et al. 2011), sollte aus arbeitsmedizinischer Sicht die Indikation zur HIV-PEP beispielsweise auch bei einer oberflächlichen Verletzung (z. B. mit chirurgischer Nadel) ohne Blutfluss u. U. in Erwägung gezogen werden und es stellt sich die Frage, ob bei einer „(blutenden) perkutanen Stichverletzung mit einer Hohlraumnadel oder einer Schnittverletzung mit kontaminiertem Skalpell bei einer Viruslast des Indexpatienten < 50 Kopien/ml“ eine HIV-PEP dem betroffenem Beschäftigten nicht besser doch „empfohlen“ werden sollte, anstelle diese nur „anzubieten.“
Eine HIV-PEP hat eine hohe Effektivität und bietet bei begrenzter Therapiedauer eine einmalige Chance, eine Infektionsübertragung zu verhindern. Die Verträglich-keit der antiretroviralen Medikation im Rahmen einer PEP bei HIV-negativen Mitarbeitern unterscheidet sich jedoch oftmals von der Verträglichkeit im Rahmen einer HIV-Behandlung. In einer prospektiv beobachtenden Studie zu Nadelstichverletzungen (NSV) am Universitätsklinikum Frankfurt gaben beispielsweise 58,5 % der Mitarbeiter an, dass sie die PEP schlecht vertragen hätten, 31,7 % bewerteten die Verträglichkeit der PEP als „mäßig“ (Himmelreich et al. 2013). Vor- und Nachteile der HIV-PEP sind deswegen stets in der Zusammenschau aller Befunde und Konstellationen abzuwägen.
Empfohlene Basis- und Kontrolluntersuchungen
Diese werden gemäß der neuen Leitlinie in Tabelle 2 dargestellt (DAIG 2013, s. „Weitere Infos“).
Bei den Blutuntersuchungen nach NSV sind aus arbeitsmedizinischer Sicht jedoch auch folgende Punkte zu bedenken:
Hepatitis C (HCV): Bei HCV-positivem Indexpatienten sollte bei dem betroffenen Mitarbeiter eine HCV-PCR nach 2–4 Wochen und falls diese negativ ist erneut nach 6–8 Wochen durchgeführt werden (Sarrazin et al. 2010).
Die Tabelle impliziert u. U., dass eine HCV-Nachuntersuchung nicht erforderlich ist („falls indiziert/falls Exposition vorlag“ s. oben) – vor dem Hintergrund der langen Inkubationszeit von HCV erscheint dies nicht angemessen; die Inkubationszeit kann 2–26 Wochen betragen, liegt aber in der Regel bei 7–8 Wochen.
Hepatitis B (HBV): Nach einer NSV gilt es zu klären, ob der betroffene Mitarbeiter eine ausreichende Hepatitis-B-Immunität aufweist. Das Vorgehen sollte nach den Empfehlungen der STIKO zur postexpositionellen Hepatitis-B-Immunprophylaxe (PEP) erfolgen. Die anti-HBc-Bestimmung vor HBV-Impfung ist nur in Ausnahmefällen indiziert. Bei einem nicht ausreichenden HBV-Impfschutz ist u. U. die Gabe von Immunglobulinen indiziert, eine alleinige Impfung (Erläuterung der Tabelle 2) ist, sofern das Anti-HBs nie 100 IE/l war oder unbekannt ist, nicht ausreichend (STKO 2013).
HIV: Die amerikanische Leitlinie sieht bei der Verwendung eines 4. Generation HIV-Test mit gleichzeitigen Nachweis von HIV p24-Ag keine 6-Monats-Kontrollen mehr vor. Stattdessen erfolgt eine Kontrolle nach 6 Wochen und nach 4 Monaten erfolgt der Abschluss der HIV-Kontrollen (Kuhar et al. 2013; New York State Department of Health 2012).
Neuere Studien zeigen, dass neben den infektiologischen Gefährdungen auch psychosomatische/psychiatrische Erkrankungen im Anschluss an eine NSV auftreten können. Ein schnellstmöglich mitgeteiltes negatives Testergebnis entlastet den Beschäftigten und spart überdies Kosten.
Es wäre aus diesen Gründen wünschens-wert, wenn die Unfallversicherungsträger ihr Regeluntersuchungsprogramm nach Stich- und Schnittverletzungen überarbeiten und dem aktuellen Stand der Technik und den methodischen Verbesserung anpassen würden.
Untersuchung des Indexpatienten
In der neuen Leitlinie finden sich folgende Zitate:
- „Das Einverständnis zur Durchführung des HIV-Tests und der Hepatitis-Serologie muss vorliegen, bevor diese Untersuchungen durchgeführt werden. Eine Ablehnung des HIV-Testes durch die Indexperson ist zu respektieren.“
- „Die größte Schwierigkeit und Herausforderung bei der Indikationsstellung für die HIV-PEP ist die Abschätzung des Infektionsrisikos in Fällen, in denen der Sero- bzw. der Infektionsstatus der Indexperson unbekannt ist.“
Die Testung des Indexpatienten nach einer NSV ist die Voraussetzung für eine optimale Betreuung des betroffenen Mitarbeiters. In dem Moment, in dem sich der Mitarbeiter sticht, wird er selbst zum Patienten und sollte eine bestmögliche Behandlung bekommen. Die Kenntnis des Infektionsstatus des Indexpatienten ermöglicht eine individuelle Therapie und verhindert bei negativem HIV-Testergebnis etwaige eventuell schwerwiegende Nebenwirkungen einer HIV-PEP.
Im klinischen Alltag besteht oftmals Unsicherheit inwieweit der Patient zur Blutuntersuchung verpflichtet werden kann, um Schaden für den betroffenen Mitarbeiter abzuwenden. Aus interdisziplinärer Sicht erscheint uns die Testung des Indexpatienten angemessen und im Allgemeinen rechtmäßig (Wicker et al. 2008).
Sonstiges
In der neuen Leitlinie steht, dass bei NSV beim Umgang mit Klinikabfall eine HIV-PEP nicht empfohlen wird.
Hier bedarf es jedoch aus arbeitsmedizinischer Sicht einer individuellen Gefährdungsbeurteilung des stattgehabten Unfalls und der Infektionswahrscheinlichkeit. Verletzt sich beispielsweise eine Reinigungskraft im Krankenhaus an einer Kanüle, die aus Unachtsamkeit in einen Müllbeutel geworfen wurde, und findet diese NSV beispielsweise auf einer infektiologischen Station statt, sollte man selbstverständlich zu einer HIV-PEP raten.
Literatur
Cohen MS, Chen YQ, McCauley M et al.: Prevention of HIV-1 Infection with early antiretroviral therapy. N Engl J Med 2011; 365: 493–505.
Himmelreich H, Rabenau HF, Rindermann M, Ste-phan C, Bickel M, Marzi I, Wicker S: Management von Nadelstichverletzungen. Dtsch Arztebl Int 2013; 110: 61–67.
Kuhar DT, Henderson DK, Struble KA et al.: US Public Health Service Guideline: Updated US Public Health Service Guidelines for the Management of occupational exposures to Human Immunodeficiency Virus and recommendations for postexposure pro-phylaxis. Infect Control Hosp Epidemiol 2013; 34: 875–892.
Sarrazin C, Berg T, Ross RS et al.: Update der S3-Leitlinie Prophylaxe, Diagnostik und Therapie der Hepatitis-C-Virus (HCV)-Infektion, AWMF-Register-Nr.: 021/012. Z Gastroenterol 2010; 48: 289–351.
Wicker S, Gottschalk R, Spickhoff A, Rabenau HF: HIV-Test nach Nadelstichverletzung: Muss der Index-patient zugestimmt haben? Dtsch Med Wschr 2008; 133: 1517–1520.
Weitere Infos
DAIG. Deutsch-Österreichische Leitlinien zur Postexpositionellen Prophylaxe der HIV-Infektion
New York State Department of Health AIDS Institute; HIV prophylaxis following occupational exposure
https://www.ahrq.gov/gam/index.html
STIKO: Mitteilung der Ständigen Impfkommission (STIKO) am Robert Koch-Institut (RKI). Epidemiologisches Bulletin 2013; 34: 313–344
https://www.rki.de/DE/Aktuelles/Publikationen/publikationen-node.html?__blob=publicationFile
Autorin
Prof. Dr. med. S. Wicker
Universitätsklinikum Frankfurt
Betriebsärztlicher Dienst
Theodor-Stern-Kai 7
60590 Frankfurt