Abstract / Zusammenfassung
Humoral immune response of vaccinated individuals during the COVID-19 pandemic
With increasing infection pressure, the seroprevalence of antibodies against the nucleocapsid antigen of SARS-CoV-2 in a group of vaccinated study participants has increased significantly compared to our previous study in 2021 and is currently 29.6%. The congruence between a positive RT-PCR test and the detection of anti-nucleocapsid antibodies is high at 95.23%. The rate of infections not detected or unnoticed with an RT-PCR test was low and only one case could be proven exclusively serologically.
In principle, it can be assumed that all study participants have reached a high level of immune protection induced by the vaccination. Regardless of the vaccination scheme, almost all people have protection-relevant antibody titers against the spike protein of the SARS-CoV-2 virus, even more than 300 days after vaccination.
Keywords: SARS-CoV-2 – seroprevalence – spike protein – nucleocapsid protein – undetected cases
doi:10.17147/asu-1-225877
ASU Arbeitsmed Sozialmed Umweltmed 2022; 57: 656–660
Humorale Immunantwort von geimpften Personen
im Verlauf der COVID-19-Pandemie
Mit steigendem Infektionsdruck ist in einer Gruppe von geimpften Studienteilnehmenden die Seroprävalenz mit Antikörpern gegen das Nucleocapsid-Antigen von SARS-CoV-2 gegenüber der Voruntersuchung im Jahre 2021 deutlich angestiegen und liegt derzeit bei 29,6 %. Die Übereinstimmung zwischen positivem RT-PCR-Test und dem Nachweis von anti-Nucleocapsid-Antikörpern ist mit 95,23 % hoch. Die Rate an mit einem RT-PCR Test nicht erkannten beziehungsweise unbemerkten Infektionen war niedrig und nur ein Fall konnte ausschließlich serologisch nachgewiesen werden.
Grundsätzlich ist von einem hohen, durch die Impfung induzierten Immunschutz aller Studienteilnehmenden auszugehen. Unabhängig von den Impfschemata liegen bei fast allen Personen auch nach über 300 Tagen nach der Impfung schutzrelevante Antikörper-Titer gegen das Spike-Protein des SARS-CoV-2-Virus vor.
Schlüsselwörter: SARS-CoV-2 – Seroprävalenz – Spikeprotein – Nukleokapsidprotein – Dunkelziffer
Einleitung
Nach der Identifizierung des neuartigen Coronavirus SARS-CoV-2 Anfang Januar 2020 entwickelte sich eine weltweite Pandemie, die sich derzeit im dritten Jahr befindet und bisher über 6 Mio. Todesfälle (mit-)verursacht hat (WHO 2020, 2022). Impfstoffe gegen das SARS-CoV-2 waren in Deutschland erst ab Dezember 2020 verfügbar und deren Anzahl zunächst begrenzt. Viele Beschäftigte konnten jedoch im Verlauf der beginnenden Impfkampagne zeitnah geimpft werden. Bei einigen Personenkreisen, die vergleichsweise früh geimpft wurden, kam es allerdings zu unterschiedlichen Impfschemata: Initial wurden auch heterologe Impfschemata verwendet, bei denen in den meisten Fällen nach der Erstgabe von Vaxzevria® (Astra Zeneca) ein mRNA-Impfstoff als Zweitimpfung appliziert wurde. Später fanden nur noch homologe Impfschemata mit mRNA-Impfstoffen Verwendung.
Um immunologische Unterschiede aus diesen Ansätzen zu identifizieren und jeweils den Impferfolg zu ermitteln, wurde bei Beschäftigten im bremischen Öffentlichen Dienst diese Studie initiiert. Nach einem positiven Votum der Ethik-Kommission der Ärztekammer Bremen (Vorlage-Nr.: 781) wurde diese Untersuchung als monozentrische, nicht-prospektive Beobachtungsstudie in das Deutsche Register klinischer Studien aufgenommen (DRKS-ID: DRKS00025567).
Die ersten Ergebnisse lagen nach einer Erhebung im Jahre 2021 vor und wurden in dieser Zeitschrift (Ausgabe 9/2021) veröffentlicht.
Bei allen Studienteilnehmenden konnte ein gutes Ansprechen auf die COVID-19-Impfung gezeigt werden. Nur wenige Teilnehmerinnen und Teilnehmer erreichten bei den anti-Spike-Antikörpern nicht den als herstellerseitig angegebenen oberen, quantifizierbaren Bestimmungsgrenzwert von mindestens 250 U/ml. Heterologe Impfschemata standen homologen Impfschemata nicht nach, da keine wesentlichen Unterschiede beobachtet wurden.
Im Zeitraum vom 11.05.2022 bis 30.06.2022 wurde eine erneute Testung der Studienteilnehmenden durchgeführt, um beurteilen zu können, wie sich die humorale Immunantwort im Verlauf der Pandemie entwickelt hat. Es galt, die Frage zu beantworten, wie hoch die initial gemessenen Antikörper-Ergebnisse bei den Studienteilnehmenden nach etwa einem Jahr waren und ob in den Ergebnissen Unterschiede zwischen heterologen und homologen Imfschemata beobachtet werden können.
Beeinflussende Faktoren waren neben möglichen Infektionen mit dem SARS-CoV-2-Virus auch weitere Impfungen (die sogenannten Boosterimpfungen), die bei Beginn der Studie im Jahre 2021 noch nicht absehbar gewesen sind. Insofern wurde das Studienprotokoll aktualisiert und erneut der Ethikkommission der Ärztekammer Bremen zur Prüfung vorgelegt. Es fanden sich weiterhin keine berufsrechtlichen oder berufsethischen Einwände gegen die Fortführung der Studie, das positive Votum blieb gültig.
Alle an der Studie teilnehmenden Personen wurden mit Impfstoffen, die sich gegen den ursprünglichen SARS-CoV-2-Wildtyp richten, geimpft. Zukünftig werden voraussichtlich zielgerichtete Impfstoffe auf Virusvarianten beziehungsweise Subtypen sowie Totimpfstoffe verfügbar sein, so dass aktuell für dieses Studienkollektiv noch eine gute Vergleichbarkeit bezüglich der Immunantworten bestand (Deutsches Ärzteblatt 2022).
Methode
Zu Beginn der Untersuchung wurden vom 14. bis 29. Juni 2021 freiwillige Studienteilnehmende (n = 103) aus dem Öffentlichen Gesundheitsdienst sowie dem Bereich der Arbeitsmedizin des bremischen Öffentlichen Dienstes in die Studie aufgenommen. Als Einschlusskriterium galt eine abgeschlossene COVID-19-Impfung, die mindestens 14 Tage und nicht länger als 3 Monate zurücklag.
Bei der aktuellen, zweiten Erhebung in der Zeit vom 11.05. bis 28.06.2022 konnten 71 Personen erneut untersucht werden. Die Quote der Wiederteilnahme lag damit bei 69 %, was durch mehrere Kontaktversuche erreicht wurde.
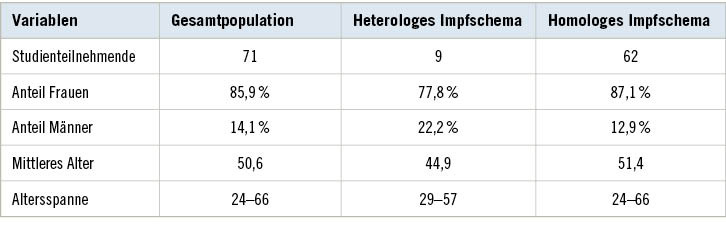
Von den verbliebenen Teilnehmenden wiesen 9 Personen ein heterologes Impfschema (Vaxzevria® und mRNA-Impfstoff) sowie 62 Personen ein homologes Impfschema (Biontech/Pfizer: 60 Personen/Moderna: 2 Personen) auf.
Die Studienpopulation war überwiegend weiblich (85,9 %; ➥ Tabelle 1); Personen mit der Geschlechtsangabe „divers“ fanden sich nicht.
Als Impfstoffe für die Wiederauffrischungsimpfungen wurden nur mRNA-Impfstoffe verwendet. Die dritte Impfung hatten bereits 62 Personen (87,3 %; Biontech/Pfizer: 49, Moderna: 13), die vierte Impfung 5 Personen (7 %; Biontech/Pfizer: 3, Moderna: 2) erhalten.
Lediglich 4 Personen haben kein weiteres Impfangebot seit Studienbeginn angenommen und wiesen nur 2 Impfungen auf (5,6 %). Immer den identischen Impfstoff hatten 44 Personen erhalten (75,8 %; nur Biontech/Pfizer: 43, nur Moderna: 1). Alle anderen Personen hatten entweder anfangs Vaxzevria® erhalten oder wurden mit jeweils verschiedenen mRNA-Impfstoffen versorgt.
Als Nachweismethode wurden zwei Testsysteme des Herstellers Roche verwendet, die entweder Antikörper gegen das Nucleocapsid-Antigen oder Antikörper gegen das Spike-Protein detektieren. Zu beachten ist, dass sich die unterschiedlichen Antikörper in der
Diagnostik ergänzten. Während Antikörper gegen das Nucleocapsid-Protein nur nach einer Infektion mit SARS-CoV-2 auftreten, sind Antikörper gegen das Spike-Antigen sowohl nach Infektion als auch nach Impfung nachweisbar. Damit war es möglich anhand der Ergebnisse bei der Studienpopulation zwischen Immunreaktion nach Infektion beziehungsweise Impfung zu unterscheiden.
Die Antikörper gegen das Spike-Antigen konnten durch das Testsystem (Elecsys® Anti-SARS-CoV-2 S) im akkreditierten Labor quantitativ angegeben werden und waren in Anlehnung an den WHO-Standard kalibriert. Die klinische Sensitivität dieser Nachweismethode wurde herstellerseitig mit 98,8 % (95%-KI: 98,1–99,3 %) und die klinische Spezifität mit 99,98 % (95%-KI: 99,91–100%) angegeben.
Die Leistungsdaten des qualitativen Antikörper-Testkits gegen das Nucleocapsid-Antigen (Elecsys® Anti-SARS-CoV-2) betrugen nach Herstellerangaben 99,5 % (95%-KI: 97,0–100 %; klinische Sensitivität ab Tag 14) sowie 99,5 % (95%-KI: 98,63–99,85 %; klinische Spezifität). Elecsys® Anti-SARS-CoV-2 weist dabei Antikörper-Titer nach, die nach Herstellerangaben nachweislich positiv mit neutralisierenden Antikörpern korrelieren (Roche 2021).
Für dieses Immunoassay zum primär eigentlich rein qualitativen Nachweis von Antikörpern gegen SARS-CoV-2 konnten laborseitig weitere Angaben gemacht werden. Dabei handelt es sich um die im Detektionsansatz gemessene Menge an Chemilumineszenz, die als relatives Maß für die Höhe der Antikörperantwort gesehen werden kann. Grundsätzlich wird bei diesem Elektro-Chemilumineszenz-Immunoassay (ECLIA) ab einem Wert über 1 das Ergebnis als positiv gewertet. Ergebniswerte die deutlich über 1 liegen weisen demnach eine höhere Menge an Antikörpern gegen das Nucleocapsid-Antigen auf.
Ergebnis

Fig. 1: Indications of the study participants (own illustration)
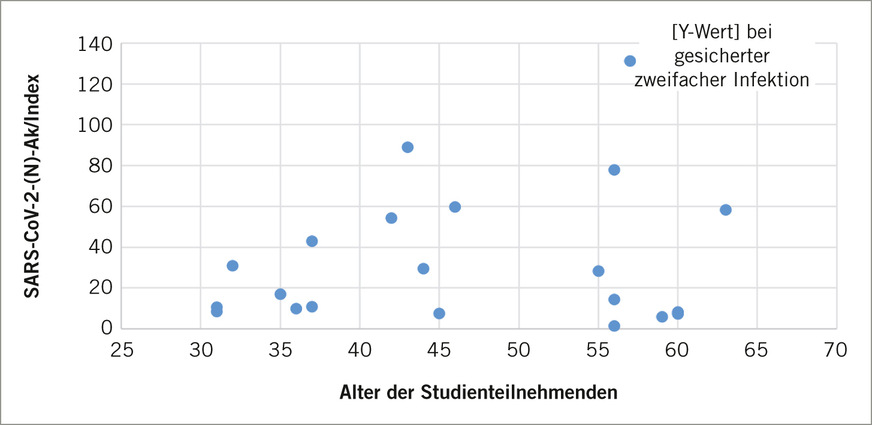
Fig. 2: Age distribution for SARS-CoV-2-(N) antibodies (own illustration)
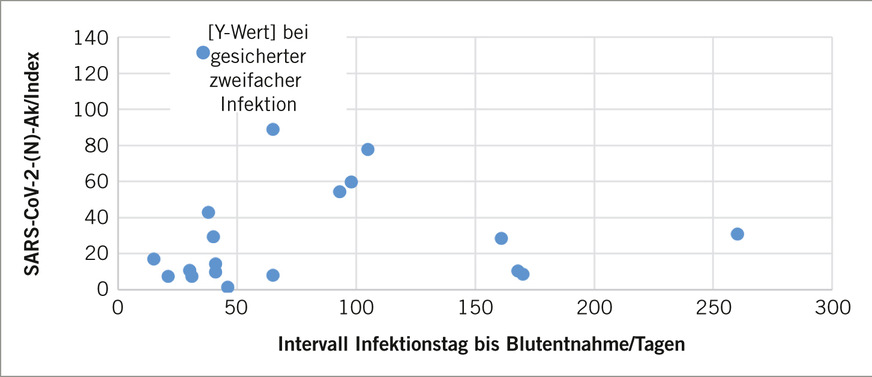
Fig. 3: Antibodies against the neucleocapsid antigen (own illustration)
Zeitgleich zu den Blutentnahmen, die zwischen 316 und 363 Tagen nach der ersten Untersuchungsserie im Juni 2021 stattfanden, wurden anamnestische Angaben der Studienteilnehmenden in Bezug auf die Risikogefährdung ermittelt. Dabei wurden der direkte Kontakt zu infizierten Personen, die regelmäßige Vornahme eines Selbsttests, das heißt mindestens 2-mal/Woche, sowie das Auftreten von SARS-CoV-2-Infektionen, das heißt eines positiven Schnelltests beziehungsweise RT-PCR-Tests, erfragt (➥ Abb. 1).
Anhand der anamnestischen Angaben ergab sich eine SARS-CoV-2-Prävalenz von 33,8 %. Allerdings gaben zwei Personen an, dass der nachfolgende RT-PCR-Bestätigungstest negativ gewesen sei, so dass die korrigierte Prävalenz 29,57 % beträgt.
In den Ergebnissen zeigte der Elecsys® Anti-SARS-CoV-2-Test eine hohe Kongruenz mit den anamnestischen Angaben bezüglich eines positiven RT-PCR-Testergebnisses. Von den 21 Studienteilnehmenden mit positiven RT-PCR-Tests konnten in 20 Fällen (95,23 %) Antikörper gegen das Nucleocapsid-Antigen nachgewiesen werden. Eine Person wies somit trotz eines berichteten positiven RT-PCR-Befundes keine anti-Nucleocapsidprotein-Antikörper auf. Des Weiteren konnten bei einer Person, die trotz regelmäßiger Selbsttests nie einen positiven Test aufwies, anti-Nucleocapsidprotein-Antikörper nachgewiesen werden. Zusammenfassend ergibt sich somit in dem Studienkollektiv eine Seroprävalenz von 29,6 %.
Bei der Gruppe der Personen mit „direkten Kontakt zu Infizierten“ lag die relative Seroprävalenz mit 51,3 % (19 von 37 Personen) jedoch deutlich höher.
In Bezug auf die Altersverteilung wurden hinsichtlich der relativen anti-Nucleocapsidprotein-Antikörperkonzentrationen keine eindeutigen Unterschiede ersichtlich (➥ Abb. 2).
Geschlechtsspezifische Aussagen sind aufgrund der geringen Studiengröße mit einem überproportionalen Frauenanteil nicht möglich. Nur zwei der zehn Männer wiesen Antikörper gegen das Nucleocapsid-Antigen auf. Ihre Werte lagen bei 6 beziehungsweise 29,5. Die Werte der infizierten Frauen (19 von 61) lagen zwischen 1,5 und 131,1.
Auf eine Besonderheit ist bei den Elecsys® Anti-SARS-CoV-2-Testergebnissen jedoch hinzuweisen: Bei einer Studienteilnehmerin konnten bereits im Jahre 2021 Antikörper gegen das Nucleocapsid-Antigen nachgewiesen werden. Diese Person hatte dann im April 2022 eine mittels RT-PCR-Test bestätigte (erneute) SARS-CoV-2-
Infektion erlitten und wies anschließend die höchste relative Antikörperkonzentration (131,1) aller Studienteilnehmenden auf.
Insgesamt scheinen die ermittelten, relativen anti-Nucleocapsidprotein-Antikörperkonzentrationen mit zunehmender Zeitspanne zwischen zurückliegender Infektion und Probennahme abzunehmen (➥ Abb. 3).
Bei den Antikörpern gegen das Spike-Antigen blieben bis auf zwei Ausnahmen und unabhängig davon, ob eine Infektion stattfand oder nicht, die Ergebnisse aller Teilnehmenden über der herstellerseitig angegebenen, oberen quantifizierbaren Bestimmungsgrenze. Damit konnten selbst über 300 Tage nach der Impfung anti-Spikeprotein-Antikörper mit Werten > 250 U/ml nachgewiesen werden. Lediglich zwei Personen erreichten nicht den maximal möglichen Wert, ihre Antikörper-Level waren leicht vermindert (238–242 U/ml).
Zusammengefasst entwickelten fast alle Studienteilnehmenden als geimpfte Personen unabhängig vom jeweiligen Impfabstand und der Anzahl der Impfungen Antikörper gegen das Spike-Antigen, die die herstellerseitig angegebene obere quantifizierbare Bestimmungsgrenze von > 250 U/ml überschritten (n = 69/97,2 %). Unterschiede zwischen homologen und heterologen Impfschemata waren damit nicht erkennbar. Alle Personen, die initial einen Vektor-Impfstoff erhielten, erreichten die herstellerseitig angegebene obere Abscheidegrenze. Auf eine Verdünnung zwecks weiterer Bestimmung des Werts über 250 U/ml hinaus wurde auch zu diesem Zeitpunkt wie bereits bei der ersten Erhebung im Jahre 2021 verzichtet.
In Bezug auf den Impfstatus der Studienteilnehmenden konnten keine klaren Unterschiede hinsichtlich des Infektionsrisikos erfasst werden. Sowohl Personen mit zwei, drei oder vier Impfungen wiesen nach initialer Seronegativität nachfolgend auf eine Infektion Antikörper gegen das Nucleocapsid-Antigen auf, wodurch jeweils eine SARS-CoV-2-Infektion trotz Impfung unterstellt werden muss (sog. Durchbruchsinfektion). Die jeweils relativen Prävalenzen für zwei, drei beziehungsweise vier Impfungen lagen in vergleichbaren Bereichen (zwei Impfungen: 25 %, drei Impfungen: 27,4 %, vier Impfungen 20 %).
Zu beachten ist allerdings, dass die Impfserie der dritten Impfung bei der Mehrzahl der Studienteilnehmenden erst in der Mitte des Beobachtungszeitraums durchgeführt wurde (Oktober 2021 bis Januar 2022). Die vierte Impfserie erfolgte in der Zeit von März bis Mai 2022, also erst gegen Ende des Studienzeitraums. Aufgrund des anamnetisch angebenden Datums des positiven RT-PCR-Tests konnte allerdings ermittelt werden, dass nur bei einer Person die Infektion vor der dritten Impfung aufgetreten war. Alle anderen Personen mit drei beziehungsweise vier Impfungen erlitten die SARS-CoV-2-Infektion nach der letzten Impfung (4–178 Tage).
In Hinblick auf die Krankheitsschwere von COVID-19 gaben die Studienteilnehmenden überwiegend milde Symptome an (86 %; ➥ Abb. 4). Kritische Erkrankungen traten nicht auf.
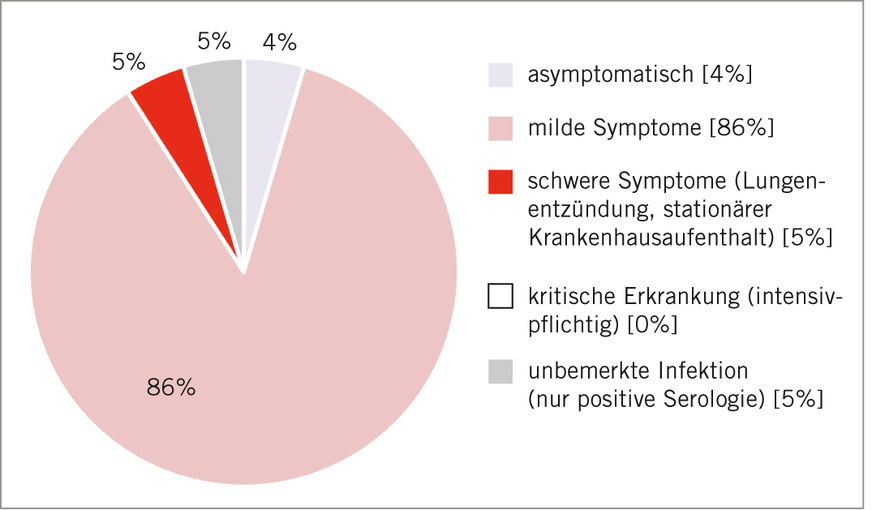
Fig. 4: Severity of illness (anamnestic) (own illustration)
Diskussion
Mit steigendem SARS-CoV-2-Infektionsdruck hat auch die Antikörper-Seroprävalenz im geimpften Studienkollektiv deutlich zugenommen. Im Vergleich zur ersten Erhebung im Juni 2021 ist die Seroprävalenz von 0,97 auf nun 29,6 % gestiegen.
Dabei zeigte sich, dass Personen mit direktem Kontakt zu Infizierten eine höhere Seroprävalenz (51,3 %) und damit ein deutlich gesteigertes Infektionsrisiko aufweisen. Auch wenn die Art und Weise des Kontakts im Studiendesign nicht konkret ermittelt wurde, kann in Bezug auf das berufliche Spektrum der Teilnehmenden davon ausgegangen werden, dass es sich mutmaßlich zu einem gewissen Anteil um berufliche Kontakte handelte, die dann entsprechend unter adäquater persönlicher Schutzausrüstung stattfanden. In anderen Studien konnte bereits gezeigt werden, dass ein höheres Infektionsrisiko je nach Tätigkeitsprofil existiert (Hildebrandt et al. 2022). In Kliniken scheint das höchste Gefahrenpotenzial bei Personal, das auf separaten COVID-19-spezifischen allgemeinen Stationen und Intensivstationen arbeitet, zu liegen (Tomczyk et al. 2022).
Da es sich bei der hier untersuchten Studienpopulation um medizinisches Personal aus dem Öffentlichen Gesundheitsdienst beziehungsweise dem Bereich der Arbeitsmedizin des bremischen Öffentlichen Dienstes handelt, kann ebenso ein höheres Infektionsrisiko als bei der Allgemeinbevölkerung angenommen werden. Leider liegen nur sehr wenige aktuelle Daten zur Seroprävalenz in Deutschland und noch weniger aus dem Land Bremen vor. Die Informationen über das Ausmaß der SARS-CoV-2-Infektionen beschränken sich weitgehend auf die Zahl der von den Gesundheitsbehörden gemeldeten COVID-19-Fälle. Insbesondere aktuelle Angaben zu Seroprävalenzen fehlen. Aus München konnte zuletzt in der „Prospektiven COVID-19-Kohorte München“ des Tropeninstituts des LMU Klinikums München eine adjustierte/gewichtete Seroprävalenz von 13,67 % angegeben werden (LMU Klinikum München 2021). Insofern scheint weiterer Forschungsbedarf zu bestehen, um die Prävalenz von SARS-CoV-2 besser beurteilen zu können. Gerade im Zusammenspiel mit der so wichtigen Impfquote könnten sich daraus Anhalte für den Immunschutz der Bevölkerung sowie die weitere Entwicklung der pandemischen Lage ergeben.
Bei den von den Studienteilnehmenden erhobenen Daten fällt auch auf, dass sich scheinbar 15 % der Kohorte nicht regelmäßig mittels Selbsttest getestet haben. Diese Aussage erstaunt, da für dieses Personal nach § 28b IfSG eigentlich eine Testpflicht vorlag. Allerdings ist diese am 20.03.2022 bei der Änderung des IfSG ersatzlos gestrichen worden, was vor dem Zeitpunkt der jetzigen Erhebung lag. Dennoch ergibt sich die Frage, ob verpflichtende Selbsttests in Zukunft ein adäquates, präventives Mittel über einen längeren Zeitraum sein können. Zudem weisen diese Schnelltests in der Praxis eine doch eher geringe Sensitivität auf (Wagenhäuser et al. 2021), was sich negativ auf die Selbsttest-Compliance beim medizinischen Personal auswirken kann.
Auffällig in dieser Untersuchung erscheint die geringe Dunkelziffer beziehungsweise die Anzahl der nicht erkannten Infektionen. Nur ein nicht durch einen RT-PCR-Test bestätigter Fall konnte serologisch detektiert werden (1,4 %), was eine sehr geringe Dunkelziffer impliziert (Faktor < 0,1). Dass mit anhaltendem Infektionsdruck auch die Rate an nicht erkannten Fällen absinkt, wurde bereits in anderen Studien beschrieben (Gornyk et al. 2021). Die hier errechnete Dunkelziffer scheint allerdings sehr niedrig zu liegen. Bundesweit werden Werte von 45 % unentdeckter Fälle vermutet, wobei mutmaßlich insbesondere in sozioökonomisch benachteiligten Bezirken höhere Werte vorliegen dürften (Neuhauser et al. 2021).
Bei den in dieser Studie ermittelten Antikörpertestergebnissen auf das Nucleocapsid-Antigen wurden individuelle Unterschiede sichtbar und es ist bereits bekannt, dass die Testergebnisse von Person zu Person sehr unterschiedlich ausfallen können (Paul-Ehrlich-Institut 2022). Das Lebensalter scheint in dieser Untersuchung eher eine geringere Rolle zu spielen und konkrete Einflussfaktoren konnten in dieser Studie nicht erfasst werden, wodurch sich weiterer Forschungsbedarf ergibt.
Sehr hohe Antikörper-Titer scheinen jedoch nach mehreren SARS-CoV-2-Infektionen aufzutreten, was zu dem in dieser Studie höchsten Wert an anti-Nucleocapsid-Antikörpern führte. Nach einer Infektion scheinen die anti-Nucleocapsid-Antikörperkonzentrationen abzusinken, was bei Infektionen ein üblicher Vorgang ist. Diese Studie liefert aber keine Aussage darüber inwieweit beziehungsweise wie lange relevante anti-Nucleocapsid-Antikörper-Titer nachweisbar sind.
Bei den anti-Spike-Antikörpern zeigte sich, dass diese relativ lange nach zwei beziehungsweise mehreren Impfungen – in dieser Studie mehr als 300 Tage – in relevanter Konzentration vorliegen. Vergleichbare Ergebnisse zeigen sich auch in anderen Untersuchungen und anti-Nucleocapsid-Antikörper scheinen vor den anti-Spike-Antikörpern abzusinken (Scheiblauer et al. 2022).
Anhand der dargestellten Ergebnisse kann jedoch weiterhin von einem guten Ansprechen aller Studienteilnehmenden auf die COVID-19-Impfungen mit Bildung von hohen Antikörpertitern ausgegangen werden. Aufgrund der vom Hersteller angegebenen hohen Korrelation der gemessenen Antikörper mit sogenannten neutralisierenden Antikörpern kann weiterhin ein guter humoraler Immunschutz der Studienteilnehmenden nach Impfung unterstellt werden.
Allerdings konnte kein besserer Immunschutz durch Mehrfachimpfung aufgezeigt werden. Die relativen Prävalenzen in den Gruppen der Zwei-, Drei- und Vierfach-Geimpften zeigten bei Limitierung hinsichtlich der Studiengröße kaum relevante Unterschiede. Ein Einfluss der Impfungen auf den Krankheitsverlauf liegt jedoch nahe, auch wenn kein Kontrollkollektiv zur Verfügung steht. Der überwiegende Anteil der infizierten Studienteilnehmenden wies nur milde Symptome auf. Dies entspricht der Beobachtung, dass trotz Impfungen sogenannte Durchbruchsinfektionen auftreten können, die dann häufig aber mild oder asymptomatisch verlaufen (Bergwerk et al. 2021).
Als weitere Limitierung dieser Studie muss die nur zweimalige Erfassung der SARS-CoV-2-Serologie genannt werden. Häufigere Erhebungen hätten durch die dadurch mögliche kleinskalige Erstellung des Titerverlaufs gegebenenfalls bessere Aussagen ermöglicht und mehr Doppeltinfektionen aufdecken können. Ebenso wurden nur wenige Gesundheitsdaten der Studienpopulation erfasst. Vorerkrankungen und bestehende immunsuppressive Therapien der Teilnehmenden wurden nicht erfragt und können damit an dieser Stelle nicht ausgeschlossen werden.
Schlussfolgerung und Fazit
Antikörper gegen das Spike-Antigen lagen bei nahezu allen Studienteilnehmenden in sehr hoher Konzentration vor, nur zwei Personen erreichten knapp nicht die herstellerseitig angegebene obere Abscheidegrenze von > 250 U/ml. Daher kann weiterhin von einem guten Ansprechen aller Teilnehmenden auf die COVID-19-Impfungen mit Bildung von hohen Antikörpertitern unabhängig von den Impfschemata ausgegangen werden.
Die Seroprävalenz ist mit steigendem Infektionsdruck in der Studiengruppe deutlich angestiegen und liegt derzeit bei 29,6 %. Die Rate an durch Schnelltests oder RT-PCR-Tests nicht erkannten beziehungsweise unbemerkten Infektionen war niedrig und nur ein Fall wurde ausschließlich serologisch nachgewiesen.
Interessenkonflikt: Die Autoren geben an, dass keine Interessenkonflikte vorliegen.
Literatur
Bergwerk M, Gonen T, Lustig Y et al.: Covid-19 breakthrough infections in vaccinated health care workers. N Engl J Med 2021; 385: 1474–1484.
Deutsches Ärzteblatt: EMA prüft Omikron-Impfstoff von Moderna (17.06.2022). https://www.aerzteblatt.de/nachrichten/135230/EMA-prueft-Omikron-Impfst… (abgerufen am 11.07.2022).
Gornyk D, Harries M, Glöckner S: SARS-CoV-2 seroprevalence in Germany.
Dtsch Arztebl Int 2021; 118: 824–831.
Hildebrandt A, Hökelekli O, Uflacker L, Rudolf H, Paulussen M, Gatermann SG: Seroprevalence of SARS-CoV-2 antibodies in employees of three hospitals of a secondary care hospital network in Germany and an associated fire brigade: Results of a repeated cross-sectional surveillance study over 1 year. Int J Environ Res Public Health 2022; 19: 2402.
Klinikum der Ludwig-Maximilians-Universität München – Abteilung für Infektions- und Tropenmedizin: KoCo19-Studie „Prospektive COVID-19 Kohorte München“. Zusammenfassung der Ergebnisse, 5. Studienrunde (31.05.2022). http://www.klinikum.uni-muenchen.de/Abteilung-fuer-Infektions-und-Trope… (abgerufen am 11.07.2022).
Neuhauser H, Schaffrath Rosario A, Butschalowsky H et al.: Germany’s low SARS-CoV-2 seroprevalence confirms effective containment in 2020: Results of the nationwide RKI-SOEP study. medRxiv 2021.11.22.21266711.
Neumann J, Zeeb H, Dotzauer A: Humorale Immunantwort nach COVID-19-Impfung. ASU Arbeitsmed Sozialmed Umweltmed 2021; 55: 574–575.
Paul-Ehrlich-Institut – Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel: Antikörper nach SARS-CoV-2-Infektion – neue Erkenntnisse über die Sensitivität und Nachweisdauer von Antikörpertests (03/2022). https://www.pei.de/DE/newsroom/pm/jahr/2022/03-antikoerper-sars-cov-2-i… (abgerufen am 11.07.2022).
Roche: ElecsysT SARS-CoV-2 Antigen Immunoassay für den qualitativen Nachweis des SARS-CoV-2-Nukleokapsid-Antigens. 2021. https://assets.cwp.roche.com/f/94122/x/14a1b18cac/elecsys-sars-cov-2-an… (abgerufen am 27.06.2022).
Scheiblauer H, Nübling CM, Wolf T et al.: Antibody response to SARS-CoV-2 for more than one year − kinetics and persistence of detection are predominantly determined by avidity progression and test design. J Clin Virol 2022; 146: 105052
Tomczyk S, Hönning A, Hermes J et al.: Longitudinal SARS-CoV-2 seroepidemiological investigation among healthcare workers at a tertiary care hospital in Germany. BMC Infect Dis 2022; 22: 80.
Wagenhäuser I, Knies K, Rauschenberger V et al.: Clinical performance evaluation of SARS-CoV-2 rapid antigen testing in point of care usage in comparison to RT-qPCR. eBioMedicine 2021; 69: 103455. https://www.thelancet.com/journals/ebiom/article/PIIS2352-3964(21)00248… (abgerufen am 11.07.2022).
World Health Organisation (WHO): Coronavirus disease 2019 (COVID-19) Situation Report – 94 (23.04.2020). https://www.who.int/docs/default-source/coronaviruse/situation-reports/… (abgerufen am 11.07.2022).
World Health Organisation (WHO): WHO Coronavirus (COVID-19) Dashboard. 2022. https://covid19.who.int/ (abgerufen am 15.07.2022).
Kontakt
Dr. med. Jan Neumann, MaHM
Performa Nord, Zentrum für Gesunde Arbeit
Arbeitsmedizinischer Dienst
Bahnhofstraße 35
28195 Bremen
jan.neumann@performanord.bremen.de
Das PDF dient ausschließlich dem persönlichen Gebrauch! - Weitergehende Rechte bitte anfragen unter: nutzungsrechte@asu-arbeitsmedizin.com.